نشر هذا المقال بالإنجليزية، في مجلة نيتشر بتاريخ 12 كانون الثاني 2021.
كان عصر يوم جمعة في آذار 2013، عندما تلقى آندي جيل المكالمة. أصيب ثلاثة أشخاص في الصين للتوّ بسلالة جديدة من إنفلونزا الطيور. وأراد الرئيس العالمي لأبحاث اللقاحات في شركة نوفارتس، رينو رابّولي، معرفة ما إذا كان جيل وزملاؤه مستعدين لاختبار تقنية اللقاح الجديدة الخاصة بهم.
قبل ذلك بعام، قام فريق جيل في مركز أبحاث نوفارتس في الولايات المتحدة في كامبريدج، ماساتشوستس، بتعبئة سلاسل من نيوكليوتيدات الحمض النووي الريبوزي (RNA) داخل كبسولات صغيرة من الدهون، تُعرف باسم الجسيمات النانوية الدهنية (LNPs)، واستخدمها لتحصين الفئران بنجاح ضد فيروس الجهاز التنفسي.[1] هل يمكنهم الآن فعل الشيء نفسه مع سلالة الإنفلونزا الجديدة؟ وهل يمكنهم فعل ذلك بأسرع ما يمكن؟
كما يتذكر جيل، رئيس مجموعة الحمض النووي الريبوزي: «قلت: نعم، بالتأكيد. فقط أرسل لنا التسلسل». بحلول يوم الاثنين، بدأ الفريق بإنشاء الحمض النووي الريبوزي، وبحلول الأربعاء، كانوا يركّبون اللقاح. مع نهاية الأسبوع، كانوا يختبرونه في الخلايا، وبعدها بأسبوع، في الفئران.[2]
تم تطوير اللقاح بسرعة فائقة.[3] حقق فريق نوفارتس في شهر واحد ما يستغرق عادةً عامًا أو أكثر. ولكن في ذلك الوقت، كانت القدرة على تصنيع الحمض النووي الريبوزي الجاهز للاستعمال لغايات العلاج محدودةً. لن يكتشف جيل وزملاؤه أبدًا ما إذا كان هذا اللقاح، والعديد من اللقاحات الأخرى التي طوروها، ستعمل على البشر. في عام 2015، باعت شركة نوفارتس نشاطها في مجال اللقاحات.
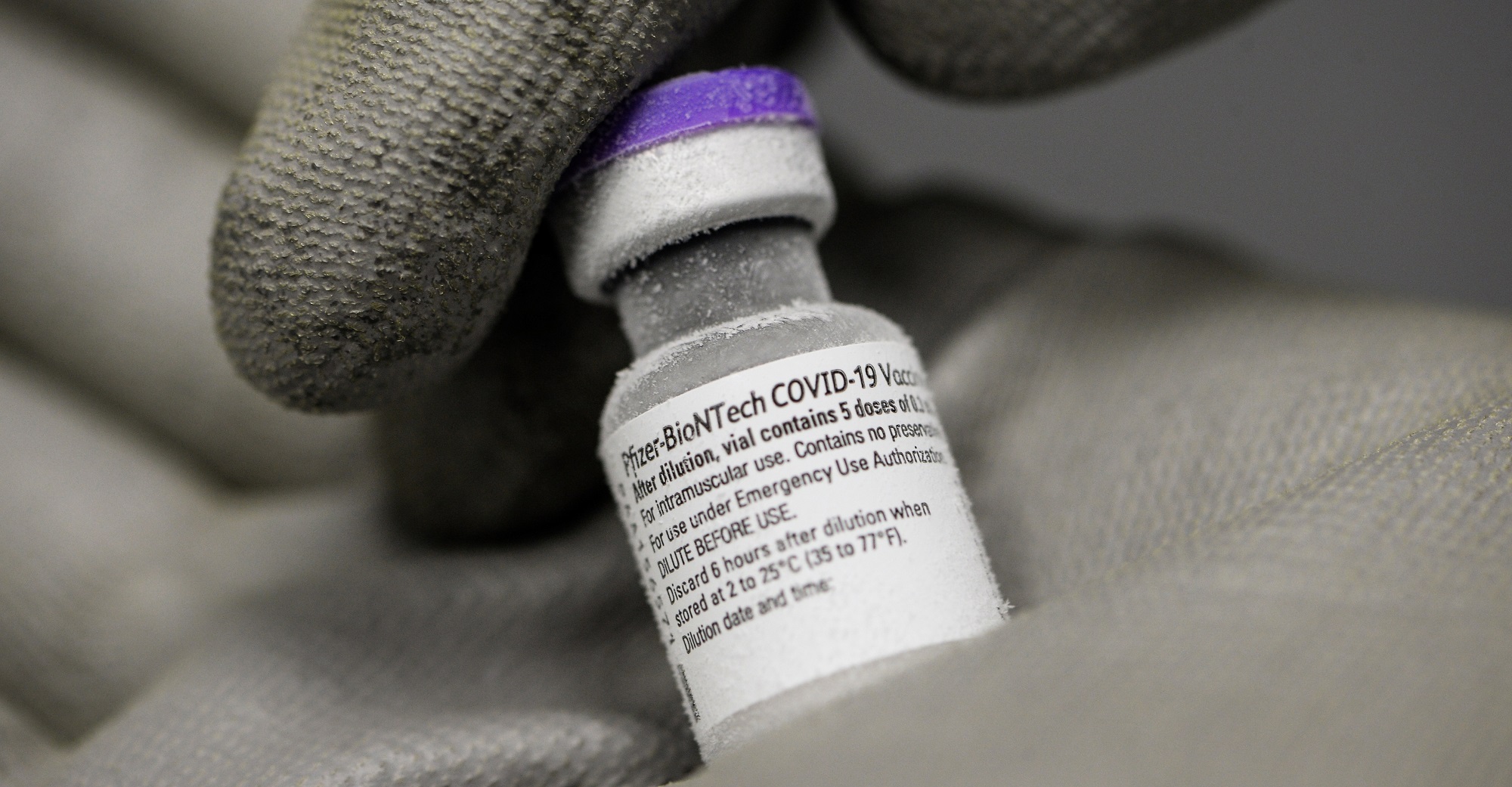
بعد خمس سنوات وجائحة عالمية، تثبت لقاحات الحمض النووي الريبوزي قيمتها. في الشهر الماضي، حصل لقاحان مرشحان من هذا النوع، أحدهما من شركة الأدوية الأمريكية العملاقة فايزر وشركة بيونتك في ماينز بألمانيا، والآخر من مودرنا في كامبريدج، ماساتشوستس، على موافقة طارئة من قبل المسؤولين في العديد من البلدان لمكافحة كوفيد-19.
لقد حان عصر لقاحات الحمض النووي الريبوزي، ودخلت العشرات من الشركات في اللعبة. ويقول جيفري أولمر، الرئيس السابق للبحث والتطوير قبل السريري، في قسم اللقاحات بشركة جلاكسو سميثكلاين (GlaxoSmithKline) في روكفيل، ميريلاند، والذي كان قبل ذلك عضوًا في فريق جيل في نوفارتيس: «إن جميع شركات الأدوية الكبرى تختبر الآن هذه التكنولوجيا بطريقة أو بأخرى».
إن فكرة استخدام الحمض النووي الريبوزي في اللقاحات موجودة منذ ما يقرب من ثلاثة عقود. تسمح التكنولوجيا الجينية، الأكثر انسيابية من الأساليب التقليدية، للباحثين بتسريع مراحل عديدة من دراسة اللقاحات وتطويرها. يمكن أن يؤدي الاهتمام الشديد الآن إلى تطوير حلول للأمراض المستعصية بشكل خاص، مثل السل وفيروس نقص المناعة البشرية والملاريا. كما يمكن أن تحسن السرعة التي يمكن تصنيعها بها لقاحات الإنفلونزا الموسمية.
لكن التطبيقات المستقبلية لهذه التكنولوجيا ستواجه بعض التحديات. المواد الخام غالية الثمن، ويمكن أن تكون الآثار الجانبية مقلقة. ويتطلب التوزيع حاليًا سلسلة تبريد مكلفة. على سبيل المثال، يجب تخزين لقاح فايزر وبيونتك الخاص بكوفيد-19 عند درجة حرارة 70 درجة مئوية تحت الصفر. ومن المرجح أن يسرّع الطابع الملحّ لكوفيد-19 حلّ بعض هذه المشاكل، لكن العديد من الشركات قد تتخلى عن الاستراتيجية بمجرد انحسار الأزمة الحالية. يبقى السؤال: أين سينتهي الأمر؟
يقول فيليب دورميتسر، رئيس أبحاث اللقاحات الفيروسية في فايزر، وزميل سابق لجيل في نوفارتس: «لقد أثبتت تكنولوجيا الحمض النووي الريبوزي نفسها، لكن تطورها لم ينته بعد. والآن بعد أن رأينا أنها فعّالة مع كوفيد-19، فمن المغري أن نرغب في فعل المزيد».
جسيمات صغيرة، تقدم كبير
تعلّم اللقاحات الجسمَ كيف يتعرف على العوامل المسببة للأمراض، ويدمرها. عادة، تُحقن مسببات الأمراض التي أُضعفت أو شظايا البروتينات أو السكريات الموجودة على أسطحها، والمعروفة باسم المستضدات أو مولدات الضد، لتدريب جهاز المناعة على التعرف على الدخيل. لكن لقاحات الحمض النووي الريبوزي تحمل فقط تعليمات إنتاج بروتينات هؤلاء الدخلاء. والهدف من ذلك، هو أن تتمكن من التسلل إلى خلايا الشخص، وحملها على إنتاج المستضدات، مما يعني تحويل الجسم إلى مصنع التلقيح الخاص به.
فكرة استخدام الحمض النووي الريبوزي في اللقاحات موجودة منذ ما يقرب من ثلاثة عقود. يمكن أن يؤدي الاهتمام الشديد الآن إلى تطوير حلول للأمراض المستعصية.
تعود فكرة التطعيم المستند إلى الحمض النووي الريبوزي إلى تسعينيات القرن الماضي، عندما استخدم باحثون في فرنسا (في شركة الأدوية سانوفي باستور (Sanofi Pasteur) حاليًا) الحمض النووي الريبوزي لأول مرة، لترميز مستضد إنفلونزا في الفئران.[4] أنتج ذلك استجابة، لكن تبين عدم إمكانية استعماله على البشر، لأن نظام توصيل الدهون الذي استخدمه الفريق شديد السمية. استغرق الأمر عقدًا آخر قبل أن تكتشف الشركات التي تبحث في علاجات تداخل الحمض النووي الريبوزي -التي تعتمد على قدرة الحمض النووي الريبوزي على منع إنتاج بروتينات معينة بشكل انتقائي- تقنيات الجسيمات النانوية الدهنية، التي تجعل لقاحات كوفيد-19 ممكنة اليوم.
يقول نيك جاكسون، رئيس البرامج والتقنيات المبتكرة في «التحالف من أجل ابتكارات التأهب للوباء» في أوسلو، وهو شراكة عالمية لتسريع تطوير اللقاحات: «أخيرًا، كان هناك تقدم. كان هذا حقًا نقطة تحول سمحت بتطبيق مرسال الحمض النووي الريبوزي على مجموعة كاملة من مؤشرات المرض المختلفة».
في عام 2012، في الوقت الذي وصف فيه جيل وزملاؤه أول لقاح مستند إلى الحمض النووي الريبوزي مغلفًا بالجسيمات النانوية الدهنية، بدأت وكالة مشروعات الأبحاث الدفاعية المتقدمة الأمريكية داربا (DARPA) في تمويل مجموعات في نوفارتيس، وفايزر، وأسترازينيكا، وسانوفي باستور، وأماكن أخرى، للعمل على لقاحات وعلاجات مستندة إلى الحمض النووي الريبوزي مشفرًا. ومع ذلك، لم تستمر أي من الشركات ذات الأسماء الكبيرة في العمل على هذه التكنولوجيا. يقول دان واتندورف، مدير برنامج سابق في «داربا»: «لقد كانوا متحفظين بشأن المجازفة بمسار تنظيمي جديد للقاحات، رغم أن البيانات بدت جيدة».
لكن شركتين صغيرتين تربطهما علاقات ببرنامج «داربا» واصلتا العمل على التكنولوجيا. إحداهما كان كيورفاك (CureVac) في توبنغن، ألمانيا، والتي بدأت اختبارات لقاح داء الكلب على البشر في عام 2013.[5] كما أن لدى كيورفاك أيضًا لقاح لكوفيد-19 في المراحل الأخيرة من الاختبار.
أما الشركة الأخرى فكانت موديرنا، التي بنت على العمل الذي مولته «داربا» لإيصال لقاح قائم على الحمض النووي الريبوزي لسلالة جديدة من إنفلونزا الطيور حتى الاختبارات السريرية في أواخر عام 2015. وقد أدت استجابات مناعية قوية بما يكفي[6] إلى دفع الشركة للمضي قدمًا في التجارب البشرية للقاحات الحمض النووي الريبوزي ضد الفيروس المضخم للخلايا (Cytomegalovirus) وهو سبب شائع للعيوب الخلقية، واثنين من الفيروسات المنقولة بالبعوض، هي شيكونغونيا (chikungunya)، وزيكا (Zika)، وثلاثة أسباب فيروسية لأمراض الجهاز التنفسي لدى الأطفال.
بدأت شركة جلاكسو سميثكلاين، التي استحوذت على معظم أصول لقاحات نوفارتس، أيضًا، بدراسة لقاح قائم على الحمض النووي الريبوزي لداء الكلب في عام 2019.
كان هذا هو المدى الكامل للتطوير السريري للقاحات الحمض النووي الريبوزي في بداية عام 2020؛ 12 لقاحًا مرشحًا فقط وصلت إلى الاختبارات على البشر، أربعة منها جرى التخلي عنها بسرعة بعد الاختبار الأولي، وواحد فقط، للفيروس المضخم للخلايا، تقدم إلى دراسة متابعة أكبر.
ثم جاء فيروس كورونا، ومعه «سُلّط هذا الضوء الهائل»، كما تقول كريستي بلوم، باحثة العلاج الجيني في جامعة ويتواترسراند في جوهانسبرج، جنوب إفريقيا. في الأشهر العشرة الماضية وحدها، دخل ما لا يقل عن ستة لقاحات قائمة على الحمض النووي الريبوزي لكوفيد-19 مرحلة الاختبارات البشرية، فيما يقترب العديد غيرها من الدراسات السريرية.
الحاجة إلى السرعة
يبدو أن لقاحات الحمض النووي الريبوزي مصممة للسرعة. من التسلسل الجيني للعامل الممرض، يمكن للباحثين سحب مقطع ترميز مستضدٍ محتمل، وإدخال هذا التسلسل في قالب حمض نووي، ثم تصنيع الحمض النووي الريبوزي المقابل قبل تعبئة اللقاح لإدخاله إلى الجسم.
تمكنت موديرنا، على سبيل المثال، من إتمام ذلك في غضون أربعة أيام بعد تلقي تسلسل جينوم فيروس كورونا المستجد. وركزت على بروتين سبايك الخاص بالفيروس، وهو بروتين سطحي يُستخدم للدخول إلى الخلايا. وبالتعاون مع المعاهد الوطنية الأمريكية للصحة، أجرت الشركة بعد ذلك تجارب إثبات الجدوى على الفئران، قبل بدء الاختبار لأول مرة على البشر، خلال فترة شهرين فقط.
يمكن لهذه التكنولوجيا أن تحدث ثورةً في الجهود المبذولة للتحصين ضد فيروس نقص المناعة البشرية، والملاريا، والإنفلونزا، وغيرها.
من الناحية النظرية، يمكن إنشاء أي لقاح بالطريقة نفسها. يقول جون شيفر، رئيس أبحاث اللقاحات وتطويرها في سانوفي باستور: «إنها حقًا منصة بهذا المعنى». باستخدام الحمض النووي الريبوزي، «ليس عليك إعادة إنشاء العملية بأكملها».
على النقيض من ذلك، تتطلب الأساليب التقليدية لإنشاء اللقاح خطوات مخصصة ومكلفة وتستغرق وقتًا طويلًا لكل مرشح. تساعد أوجه القصور هذه في تفسير سبب وجوب اختيار السلطات الصحية للسلالات التي يجب وضعها في لقاح الإنفلونزا الموسمية كل عام قبل أشهر من موسم الإنفلونزا. وغالبًا ما تخطئ هذه الاختيارات، ولا يوجد وقت للعودة واختبار بديل. نتيجة لذلك، نادرًا ما تكون فعالية لقاحات الإنفلونزا أعلى من 60%.
أما مع الحمض النووي الريبوزي، يمكن لصانعي اللقاح أن يتحولوا بسرعة أكبر إلى خيارات فعالة من المستضدات. «يمكنك نظريًا التحرك بسرعة كبيرة لضبط التسلسل ومعالجة ذلك، تقريبًا في نفس اللحظة»، بحسب رون رينو، الرئيس التنفيذي لشركة ترانسليت بيو (Translate Bio)، وهي شركة تركز على الحمض النووي الريبوزي، في ليكسينغتون، ماساتشوستس، وتعمل مع سانوفي باستور على لقاحات تستند إلى الحمض النووي الريبوزي للإنفلونزا وكوفيد-19 والعديد من مسببات الأمراض الفيروسية والبكتيرية الأخرى.
بفضل فوريّة استخدامها، يمكن للقاحات الحمض النووي الريبوزي أن تساعد في البحث الأساسي. يقوم جاستن ريتشنر، عالم اللقاحات في كلية الطب بجامعة إلينوي في شيكاغو، بتطوير لقاح يعتمد على الحمض النووي الريبوزي لحمّى الضنك في مختبره. يقوم ريتشنر وزملاؤه بشكل روتيني بقطع وتغيير تسلسل الجينات الذي يشفّر بروتين الغلاف الذي يستخدمه فيروس حمى الضنك لشن هجومه على الخلايا البشرية. من خلال تكرار تصميمهم، اختبر الباحثون حوالي 15 لقاحًا مرشحًا في الفئران.
يقول ريتشنر: «من السهل حقًا التلاعب في تسلسل ترميز اللقاح لتجربة فرضيات واستراتيجيات جديدة قد تؤدي إلى إنتاج لقاحات أفضل».
مكاسب أخرى
تساعد التطورات في التكنولوجيا الآن الباحثين على الاقتراب من بعض اللقاحات التي سُعي إليها طويلًا، مثل لقاح الإنفلونزا الشامل الذي من شأنه أن يعمل ضد أي سلالة من الفيروس دون إعادة تصميمه كل عام. ويتطلع آخرون إلى حملات ضد فيروس نقص المناعة البشرية وغيره من الأمراض الأكثر فتكًا في البلدان منخفضة الدخل. غالبًا ما استعصت مثل هذه اللقاحات على العلماء بسبب الطريقة التي تُغيّر بها مسببات الأمراض بروتيناتها السطحية بشكل منهجي لتفادي تعرف الجهاز المناعي عليها. وبعض العوامل المعدية، مثل الملاريا، لها أيضًا دورات حياة معقدة تزيد من تعقيد عملية انتقاء المستضدات.
يمكن أن تتضمن لقاحات الحمض النووي الريبوزي تعليمات لمستضدات متعددة، إما مدمجة معًا في شريط واحد، أو مع العديد من الأحماض النووية الريبوزية المعبأة معًا في جسيم نانوي واحد.
اتبع نوربرت باردي، عالم اللقاحات في كلية بيرلمان للطب بجامعة بنسلفانيا في فيلادلفيا، النهج الأخير في لقاح الإنفلونزا التجريبي الخاص به. يتكون اللقاح المتعدد من أربعة شرائط من الحمض النووي الريبوزي، كل منها يشفر بروتينًا مختلفًا للإنفلونزا، وقد نجح في حماية الفئران من الإصابة بنوع فرعي معين من فيروس الإنفلونزا.[7]
الآن، يأمل باردي وزملاؤه في مدرسة إيكان للطب في ماونت سيناي في مدينة نيويورك، تكرار التجربة على نوعين فرعيين آخرين من الفيروسات، قبل وضع كل شيء معًا في لقاح إنفلونزا مكون من 12 شريطًا، يمكن أن يحل محل الحاجة إلى التطعيم السنوي . يقول باردي: «إذا أصبت الفيروس في نقاط متعددة، يمكنك إحداث استجابات مناعية وقائية على نطاق واسع».
الاستقرار والأمان
رغم مزاياها العديدة المحتملة، فإن هناك مجالًا لتحسين تقنية لقاح الحمض النووي الريبوزي الحالية. يقول روبن شاتوك، عالم المناعة في إمبريال كوليدج لندن: «لا تزال هذه التكنولوجيا حديثة للغاية، وسنرى أجيالًا وتكرارات متعددة خلال السنوات القادمة، كما أظن».
أولًا، هناك مشكلة التخزين البارد. يتطلب لقاحا فايزر وبيونتك، وموديرنا درجات حرارة باردة جدًا للحفاظ على سلامة الحمض النووي الريبوزي الخاص بهما.
ولكن هناك شركتين على الأقل تدعيان أن لديهما لقاحات كوفيد-19 مستقرة لشهور في درجات حرارة أكثر دفئًا.
يحاكي الحمض النووي الريبوزي المتضاعف بشكل وثيق العدوى الفيروسية الطبيعية، مما يؤدي إلى استجابة مناعية أقوى وأوسع نطاقًا، وهو ما قد يسمح بأنظمة التلقيح بجرعة واحدة.
تطوي كيورفاك، التي تستخدم تقنيات الجسيمات النانوية الدهنية نفسها مثل فايزر وبيونتك، الحمض النووي الريبوزي الخاص بها في هياكل مدمجة ثلاثية الأبعاد، مما يسمح بالتخزين في درجات حرارة مبردة لعدة أشهر، كما تقول ماريولا فوتين-مليكزك، كبيرة مسؤولي التكنولوجيا. وركزت شركة سوتشو أبوجين بيوسينس (Suzhou Abogen Biosciences)، وهي شركة صينية لديها لقاح لكوفيد-19 في بداية مرحلة الاختبار على البشر حاليًا، على جودة ونقاوة الجسيمات النانوية الدهنية لإنشاء منتج يحافظ على فعاليته لمدة تصل إلى أسبوع واحد في درجة حرارة الغرفة، بحسب التقارير.[8]
وهناك تحدٍ آخر، حتى الآن، فإن لقاحات الحمض النووي الريبوزي التي تم اختبارها للاستخدام البشري ضد الأمراض، أو كوفيد-19، أو غيرها، تتطلب عمومًا جرعة مضاعفة لتكون فعالة. واستنادًا إلى ضعف الالتزام بلقاحات أخرى متعددة الجرعات، فإن العديد من الأشخاص الذين يتلقون الجرعة الأولى لن يرجعوا لتلقي الثانية على الأغلب.
يمكن لأنظمة الإيصال الجديدة إصلاح ذلك. في فاكسيس تكنولوجيز (Vaxess Technologies) في كامبريدج، ماساتشوستس، على سبيل المثال، طوّر باحثون رقعة جلد مرصعة بإبر دقيقة صغيرة قابلة للذوبان، وذات رأس حريري، يمكن ارتداؤها؛ تُقطّر ببطء اللقاح في الجسم.
كما يمكن أن يساعد إعطاء اللقاح في قطرات بدلًا من الكل مرة واحدة في حل عيب ثالث، وهو الآثار الجانبية. الاستجابات الشديدة، رغم أنها عابرة، تبدو أكثر شيوعًا مع حقن كوفيد-19 مقارنة بالتطعيمات الأخرى؛ أكثر من 80% من الأشخاص الذين تلقوا لقاح موديرنا في التجارب السريرية كان لديهم نوع من رد الفعل الشامل تجاه الحقنة، مع نوبات من التعب وآلام العضلات وغيرها من المشكلات التي غالبًا ما ثبت أنها منهكة لفترة وجيزة.
قد تكون هذه الآثار الكريهة مقبولة في خضم جائحة عالمية مميتة، كما يقول عالم اللقاحات ستانلي بلوتكين، الذي يستشيره العديد من مصنّعي اللقاحات. لكن قد يتردد الناس في الشعور بشكل روتيني بالمرض بسبب لقاح الإنفلونزا السنوي مثلًا. وبالنسبة لأي لقاحات موجهة للرُضّع، «قد يرغب المرء بالتأكيد في الحصول على شيء يسبب قدرًا أقل من ردود الفعل».
يُعتقد أن الملوثات في تركيب اللقاح ونظام توصيل الجسيمات النانوية الدهنية هما من المصادر الرئيسية للاستجابة. أنظمة التنقية لا تفي بالغرض، ولا يمكن تحسين الجسيمات النانوية الدهنية كثيرًا. لهذه الأسباب، غالبًا ما يقوم مصنعو اللقاحات بإعطاء جرعات أقل للحد من تعرض الشخص لكليهما. مع لقاح الحمض النووي الريبوزي التقليدي، فإن الجرعات المنخفضة تعني فعالية أقل. لكن شركات مثل أركتوروس ثربيوتكس (Arcturus Therapeutics) في سان دييغو، كاليفورنيا، وفاكس إكوتي (VaxEquity) في لندن، ابتكرت حلولًا بديلة من خلال إنشاء تركيبات من الحمض النووي الريبوزي ذاتية التضخيم للقاحات كوفيد-19.
بجرعات صغيرة
على عكس اللقاحات الأشهر التي تعتمد على الحمض النووي الريبوزي، والتي تحتوي على أكثر بقليل من تسلسل ترميز لبروتين سبايك الخاص بفيروس كورونا المستجد، محاطًا بمناطق تنظيمية على كلا الطرفين، فإن هذه اللقاحات المرشحة ذاتية التضاعف، تتضمن أيضًا تعليمات للحمض النووي الريبوزي لنسخ نفسه.
قد تواجه لقاحات الحمض النووي الريبوزي مصاعب مالية. لا يتوقع العديد من المطلعين على الصناعة أن يستمر الاهتمام الحالي الشديد بمجرد انحسار الوباء.
تعتبر تركيبات اللقاح أكثر صعوبة؛ تتطلب مزيدًا من تحسين التسلسل وإتقان التصنيع. لكنها تسمح للشركات بخفض الجرعة. كما أن الحمض النووي الريبوزي المتضاعف يحاكي بشكل وثيق العدوى الفيروسية الطبيعية، مما يؤدي إلى استجابة مناعية أقوى وأوسع نطاقًا، وهو ما قد يسمح بأنظمة التلقيح بجرعة واحدة.
حسنت بيونتك تقنية التضخيم.[9] قبل كوفيد-19، ركزت الشركة في الغالب على لقاحات السرطان. ولكن مع سمعة مثبتة، وقدرة إنتاج واسعة، وتدفق نقدي كبير متوقع من مبيعات لقاح كوفيد-19، «سيسمح لنا ذلك بالتوسع في منصة الأمراض المعدية بشكل أسرع»، كما يقول المؤسس المشارك والرئيس التنفيذي للشركة أوغور شاهين.
وبالمثل، حاولت زيفيوس فاكسينز (Ziphius Vaccines) في أوستكامب، بلجيكا، الاستفادة من زخم فيروس كورونا المستجد. الشركة التي تأسست في أيار 2019 في البداية لتطوير علاجات قائمة على الحمض النووي الريبوزي للأمراض النادرة مثل الضمور العضلي الدوشيني والتليف الكيسي، قامت بتجديد خطط تطويرها العام الماضي بعد أن بدأت العمل على لقاح لكوفيد-19 يستند إلى الحمض النووي الريبوزي ذاتي التضخم. يقول الرئيس التنفيذي كريس كاردون إن الشركة الناشئة تحاول الآن جمع 30 مليون يورو (37 مليون دولار أمريكي) لتطوير 14 برنامجًا من البرنامج قبل السريرية لمجموعة متنوعة من الأمراض المعدية.
قد تواجه لقاحات الحمض النووي الريبوزي مصاعب مالية. لا يتوقع العديد من المطلعين على الصناعة أن يستمر الاهتمام الحالي الشديد بمجرد انحسار الوباء.
يقول ناثانيال وانج، الرئيس التنفيذي لشركة ريبليكيت بيوسينس Replicate Bioscience في سان دييغو، كاليفورنيا، وهي شركة شارك في تأسيسها العام الماضي مع جيل لتطوير علاج للسرطان يستند إلى الحمض النووي الريبوزي: «من الصعب جدًا إقناع الناس بالمراهنة على هذا النوع من التكنولوجيا للقاحات في الأمراض المعدية». ورغم أن ريبليكيت أقامت بعض الشراكات الأكاديمية والتجارية حول لقاحات الحمض النووي الريبوزي لكوفيد-19 وفيروس زيكا، إلا أن هذا ليس ما تريد معظم شركات رأس المال الاستثماري تمويله، كما يقول وانج.
ومع ذلك، مع احتلال لقاحات الحمض النووي الريبوزي عناوين الصحف، كان جيل والعديد من زملائه السابقين يستذكرون أيامهم في نوفارتس. لو لم تقم الشركة ببيع وحدة اللقاحات الخاصة بها، فهل كان من الممكن أن تساعد في القضاء على تفشي الإيبولا أو زيكا في العقد الماضي؟
يقول كريستيان ماندل، الرئيس السابق للأبحاث والتطوير السريري المبكر في وحدة اللقاحات في نوفارتيس: «هناك دائمًا القليل من الحزن عندما ننظر إلى الوراء». لكن نجاح لقاحات كوفيد-19 اليوم يلّطف ذلك، «أنا فخور جدًا بأننا قدمنا مساهمة قيمة».
-
الهوامش
[1] Geall, A. J. et al. Proc. Natl Acad. Sci. USA 109, 14604–14609 (2012).
[2] Hekele, A. et al. Emerg. Microbes Infect. 2, e52 (2013).
[3] Ulmer, J. B., Mansoura, M. K. & Geall, A. J. Expert Opin. Drug Discov. 10, 101–106 (2015).
[4] Martinon, F. et al. Eur. J. Immunol. 23, 1719–1722 (1993).
[5] Alberer, M. et al. Lancet 390, 1511–1520 (2017).
[6] Feldman, R. A. et al. Vaccine 37, 3326–3334 (2019).
[7] Freyn. A. W. et al. Mol. Ther. 28, 1569–1584 (2020).
[8] Zhang, N.-N. et al. Cell 182, 1271–1283 (2020).
[9] Beissert, T. et al. Mol. Ther. 28, 119–128 (2020).